Терапія цервікальної неоплазії на тлі бактеріального вагінозу
Мета дослідження: оцінити ефективність вагінального декаметоксину в період підготовки до ексцизії (конізації) шийки матки у жінок з HSIL (цервікальною інтраепітеліальною неоплазією (ЦІН) ІІ) на тлі інфікування вірусом папіломи людини (ВПЛ) високого онкогенного ризику при бактеріальному вагінозі (БВ) та використання вагінального гелю з декаметоксином і гіалуроновою кислотою для покращення репарації в післяопераційному періоді.
Матеріали та методи. Обстежено 60 жінок з HSIL (ЦІН ІІ) на тлі ВПЛ-інфікування штамами високого онкогенного ризику та БВ, яким була виконана петльова ексцизія (конізація) шийки матки. Основній групі (n = 30) напередодні хірургічного лікування призначали терапію БВ розчином декаметоксину та пероральним метронідазолом строком до 7 діб, після проведення ексцизії шийки матки застосовували вагінальний гель із декаметоксином та гіалуроновою кислотою курсом 14 діб. Група порівняння (30 пацієнток) для терапії БВ використовувала пероральний метронідазол упродовж 7 діб.
За допомогою кольпоскопії проводили візуальний контроль шийки матки. За результатами ПЛР оцінювали біоценоз піхви. Елімінацію онкогенних штамів ВПЛ оцінювали методом ПЛР.
Результати. Використання у складі комбінованої терапії HSIL (ЦІН ІІ) препаратів декаметоксину зумовлювало більш швидку та повноцінну епітелізацію ранової поверхні, ніж стандартна терапія (ВР 0,27, 95% ДІ 0,10 – 0,71, р = 0,008). Через 3 місяці після застосування препаратів декаметоксину визначалося достовірне збільшення випадків нормалізації вагінальної мікробіоти (ВР 0,30, 95% ДІ 0,09 – 0,98, р = 0,047), збільшення кількості лактобацил у вагінальному секреті (ВР 0,31, 95% ДІ 0,11 – 0,84, р = 0,02). Через 6 місяців комбінованої терапії встановлено статистично вірогідний вплив декаметоксину на елімінацію онкогенних штамів ВПЛ (ВР 0,22, 95% ДІ 0,05 – 0,94, р = 0,04). Не відзначено жодної побічної дії декаметоксину як за час проведення терапії, так і в більш пізньому періоді.
Висновки. Отримані результати свідчать про пришвидшення репаративних процесів шийки матки, вираженого протимікробного ефекту, елімінацію онкогенних штамів ВПЛ і безпечність вагінального використання декаметоксину до та після проведення петльової ексцизії шийки матки у жінок з HSIL (ЦІН ІІ) на тлі ВПЛ-інфікування штамами високого онкогенного ризику при БВ.
Ключові слова: інтрацервікальна неоплазія високого ступеня, штами високого онкогенного ризику вірусу папіломи людини, бактеріальний вагіноз, петльова ексцизія, вагінальний мікробіом, епітелізація, декаметоксин.
Наразі епідеміологічні дослідження дозволяють стверджувати, що цервікальна неоплазія та рак шийки матки (РШМ) належать до захворювань, зумовлених вірусною інфекцією [1, 8, 15]. Головним тригером патогенезу слід уважати інфікування вірусом папіломи людини (ВПЛ). ДНК ВПЛ високого ступеня онкогенного ризику (переважно 16 та 18 типів) виявляються у 65–86% випадків помірної та тяжкої цервікальної інтраепітеліальної неоплазії (ЦІН) і спричиняють близько 70% випадків РШМ [5, 7, 11, 13]. Незважаючи на сучасні методи лікування передракових захворювань, асоційованих із ВПЛ, ризик розвитку РШМ за лишається високим. Щорічно у світі діагностується близько 560 000 нових випадків РШМ, який є другим найбільш поширеним раком у жінок [1, 12, 18].
Частота прогресії ЦІН у карциному коливається від 17 до 70% [1, 6, 13]. Час, необхідний для розвитку пухлинного процесу, відрізняється, особливо в пацієнток із наявністю факторів ризику. Вважається, що для прогресії в жінок з інтрацервікальною неоплазією високого ступеня (HSIL – high grade squamous intraepithelial lesion) в цервікальних мазках в інвазивний рак потрібно від 3 до 10 років. У деяких жінок цей прихований період настільки довгий, що інвазія до кінця життя може так і не розвинутися. В інших пацієнток захворювання може маніфестувати стрімко, протягом декількох місяців [1, 7, 11].
Натепер встановлений позитивний кореляційний зв’язок між бактеріальним вагінозом (БВ) та персистенцією ВПЛ у цервікальному епітелії [3, 5, 9, 10]. БВ є найбільш яскравим проявом дисбіозу піхви, що являє собою інфекційний незапальний синдром, який формується на тлі порушення мікроекології піхви [2, 4]. Численними дослідженнями доведено вплив підвищення рН піхви з подальшим розвитком БВ на збільшення ризику розвитку ЦІН [14, 16].
З урахуванням того, що ЦІН може стати етапом до малігнізації плоского епітелію, основним клінічним завданням є запобігання прогресуванню ЦІН у РШМ. Результати, наведені в іноземних клінічних настановах, свідчать про те, що ЦІН ІІ та ЦІН ІІІ слід розглядати лише з позиції хірургічного лікування. У сексуально активних дівчат-підлітків і молодих жінок кількість випадків спонтанної регресії процесу цервікальної неоплазії низького ступеня (LSIL – low grade squamous intraepithelial lesion) (ВПЛ/ЦІН I) варіює від 60–70% у перший рік, після трьох років може досягати 90%. Приблизно в 15% зміни зберігаються довше, у 30% жінок вони прогресують у тяжкий ступінь (HSIL) та у близько 1% – в інвазивну карциному. У перші 2–3 роки з моменту інфікування може спостерігатися спонтанна регресія, тому ексцизійні методи лікування неприйнятні як стартова терапія таких пацієнток [5, 17].
Також варто відмітити небезпеку недооцінювання ступеня тяжкості ураження шийки матки (ШМ) згідно з цитологічним дослідженням за наявності важчих уражень у хворих. Так, серед пацієнток із LSIL у 26% випадків виявлено ЦІН II і в 5% – ЦІН III [11]. Оскільки у 12–25% ВПЛ-позитивних жінок із ЦІН І протя гом 4 років може відбутися прогресія ЦІН, за відсутності ефекту від консервативної терапії в таких пацієнток упродовж 2 років рекомендовані хірургічні методи лікування [1, 5, 6, 8].
Необхідною умовою проведення оперативного втручання на статевих органах є відсутність запального процесу. При великому арсеналі запропонованих останніми роками консервативних методів лікування домогтися повної санації та швидкої епітелізації поверхні рани вдається не завжди. Достатньо широкий спектр організмів у мікробіоті піхви усклад нює пошук надійного засобу, який би діяв на більшість ніх видів [9].
Зазначеним вище характеристикам відпові дає декаметоксин, що має виражений бакте рицидний вплив на стафiлококи, стрептококи, капсульнi бактерiї та фунгiцидну дiю на дрiжджоподiбнi гриби, протистоцидну дiю на трихомонади, вiрусоцидну дiю на вiруси. Високо активний вiдносно мiкроорганiзмiв, стiйких до антибіотикiв, декаметоксин концентруєть ся на цитоплазматичній мембрані мікробної клітини та з’єднується з фосфатидними групами ліпідів мембран, порушуючи проникність цитоплазматичної мембрани мікроорганізмів. Препарат не всмоктується слизовими оболонками та рановою поверхнею.
Мета дослідження: вивчення клінічної ефективності використання розчину декаметоксину 0,2% (препарат Декасан) в період підготовки до хірургічного втручання (розширеної петльової ексцизії ШМ) у жінок з HSIL (ЦІН ІІ) на тлі ВПЛ-інфікування штамами високого онкогенного ризику при БВ та використання вагінального гелю з декаметоксином, гіалуроновою і молочною кислотами (препарат Гінодек) для покращення репарації в післяопераційному періоді.
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕННЯ
Об’єктом для проспективного дослідження клінічного ефекту розчину Декасан та вагінального гелю Гінодек стали 60 жінок із морфологічно верифікованою ЦІН ІІ на тлі ВПЛ-інфікування штамами високого онкогенного ризику в асоціації з БВ.
Дослідження проводилось на клінічних базах кафедри акушерства і гінекології № 1 Вінницького НМУ ім. М.І. Пирогова та відповідало принципам, викладеним у Гельсінській декларації Всесвітньої медичної асоціації (ВМА) (1989), переглянутій Генеральною асамблеєю ВМА (Сеул, 2008). Учасниці дослідження надали письмову згоду на участь у ньому. Дослідження проводилося в межах НДР «Прогнозування та профілактика порушень розвитку та функції жіночої репродуктивної системи в різні вікові періоди та корекція виявлених порушень» і було затверджене комітетом із біомедичної етики Вінницького НМУ ім. М.І. Пирогова (протокол № 1 від 22 січня 2019 р.).
Обстеження всіх учасниць включало кольпоскопію, цитологічне, гістологічне і мікробіологічне дослідження. Комбіноване лікування полягало в поєднанні конізації (ексцизії) ШМ та поетапного медикаментозного лікування з використанням перед оперативним втручанням (1 етап) антисептика Декасан (з метою передопераційної санації). На другому етапі з 10–14 дня після операції (після відходження струпа) застосовувався вагінальний гель Гінодек.
Залежно від умов дослідження жінки були розподілені на дві рівні клінічні групи:
• Основна (перша) клінічна група (n = 30), у якій пацієнткам із ЦІН ІІ напередодні хірургічного лікування призначали терапію БВ із використанням розчину Декасан та перорального метронідазолу терміном до 7 діб. На 10–14 добу після проведення ексцизії ШМ застосовували вагінальний гель Гінодек 5 мл курсом 14 діб.
• Групу порівняння (другу) становили 30 пацієнток, яким для терапії БВ призначали пероральний метронідазол протягом 7 діб. Після хірургічного втручання на ШМ була застосована стандартна терапія, що не передбачала використання гелю з декаметоксином.
Критерії включення до дослідження:
• згода та можливість узяти участь у дослідженні;
• вік від 25 до 50 років;
• наявність ЦІН ІІ (із гістологічною верифікацією);
• ВПЛ-інфікування штамами високого онкогенного ризику.
Критерії виключення та припинення участі в дослідженні:
• клінічне підтвердження інфекційного або запального процесу в ділянці оперативного втручання;
• наявність інфекційного процесу в організмі хворої, що може зумовити інфікування рани;
• цукровий діабет;
• ВІЛ-інфекція, СНІД;
• імуносупресивні стани, не пов’язані з ВІЛ/СНІД;
• вік молодше за 25 та старше за 50 років.
Всім жінкам було рекомендовано не застосовувати спринцювання, інтравагінальні або системні протимікробні препарати, крім призначеної терапії, а також обов’язково утримуватися від статевого життя в післяопераційному періоді.
1. Першочергові критерії оцінки ефективності:
• візуальна оцінка стану слизової: стан епітелію, ранової поверхні, наявність/відсутність запального/некротичного процесу;
• відсутність анормальних результатів цитологічного дослідження епітелію ШМ;
• елімінація онкогенних штамів ВПЛ.
2. Другорядні критерії оцінки ефективності:
• оцінка біоценозу піхви згідно з результатами полімеразної ланцюгової реакції (ПЛР).
3. Критерії оцінки безпеки:
• побічні ефекти, пов’язані із застосуванням вагінальних препаратів, що містили декаметоксин.
Комплексне обстеження пацієнток включало розширену кольпоскопію, дослідження мікрофлори вагінального вмісту мікроскопічним методом (забарвлення за Грамом). Тестування на ВПЛ високого канцерогенного ризику (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 66, 68 типів) проводили методом ПЛР із типоспецифічними праймерами. Діагноз БВ верифікували за діагностичними критеріями Амселя (1984), вагінальний мазок оцінювали за критеріями Ньюджента (1991).
Первинний огляд після лікування проводили через 1 місяць у першу фазу менструального циклу. Через три місяці всім пацієнткам було проведено кольпоскопію, бактеріологічне (ПЛР) та цитологічне дослідження. Остаточний огляд виконували через 6 місяців після терапії (кольпоскопія, цитологічне дослідження та ВПЛ-тестування).
При аналізі результатів лікування ЦІН ІІ оцінювали:
• повний ефект – наявність завершеного процесу епітелізації, що характеризується кольпоскопічними ознаками багатошарового плоского епітелію на всій поверхні екзоцервікса через 1 місяць після лікування;
• відсутній або неповний ефект – наявність неповної епітелізації ШМ або збереження патологічної ділянки меншого діаметра протягом 3 місяців після констатації неповного ефекту;
• рецидив – повторна поява того самого захворювання ШМ через 3 та більше місяців після досягнення повного ефекту.
Варіаційно-статистична обробка результатів дослідження була виконана за допомогою програм SPSS Statistics 22 і StatSoft Statistica 13 із визначенням основних варіаційних показників: середня величина (М), середня похибка (m), середньоквадратичне відхилення (р). При різних видах статистичного аналізу критичне значення рівня значущості приймали рівним 0,05.
РЕЗУЛЬТАТИ ДОСЛІДЖЕННЯ ТА ЇХ ОБГОВОРЕННЯ
Серед учасниць дослідження 12 (40,0%) пацієнток 1 групи та 14 (46,7%) 2 групи відзначали виділення з піхви. Більшість пацієнток (18 (60,0%) та 17 (56,7%) з 1 та 2 групи відповідно) звертали увагу на неприємний запах виділень, що з’являється або посилюється під час менструації. Дискомфорт у піхві турбував 8 (26,7%) та 9 (30,0%) обстежених 1 та 2 групи відповідно.
У всіх пацієнток були виявлені ВПЛ високого онкогенного ризику: 16 та 18 тип у 50 (83,3%) жінок, 33 тип – у 15 (25,0%), 58 тип – у 10 пацієнток (16,7%), у 8 (3,3%) була виявлена асоціація 16 і 18 типів та вагінальний дисбіоз (БВ). При цьому більш ніж у половини жінок перебіг захворювання був безсимптомним, що відзначають й інші дослідники [13]. Це підтверджує точку зору, що жінки з HSIL мають більш різноманітну мікробіоту, ніж жінки без ЦІН [14, 18].
При аналізі структури мікробіоценозу піхви нормоценоз не був виявлений. У всіх жінок визначалося підвищення рН піхвового середовища понад 4,5. При мікроскопії мазків, забарвлених за Грамом, «ключові» клітини як патогномонічна ознака БВ були виявлені у 54 (90,0%) пацієнток. При ПЛР-тестуванні відзначалися характерні зміни якісного складу мікрофлори: відсутність морфотипів лактобацил, заміна їх на асоціації Gardnerella vaginalis/Prevotella bivia/ Porphyromonas spp./Atopobium vaginae.
Отже, полімікробна структура збудників БВ була асоційована в низці випадків з облігатно-анаеробними та факультативно-анаеробними мікроорганізмами.
Через 1 місяць після проведеної ексцизії ШМ візуально відмічалося зменшення зони набряку та гіперемії в пацієнток основної групи. В основній клінічній групі (пацієнтки з ЦІН ІІ) повна епітелізація відзначалася у 26 жінок (86,7%), яким проводили санацію розчином декаметоксину 0,2% напередодні хірургічного втручання і застосовували гель з декаметоксином та гіалуроновою кислотою після операції (табл. 1).
Таблиця 1. Візуальна оцінка стану слизової ШМ через 30 діб від початку лікування, абс. ч./%
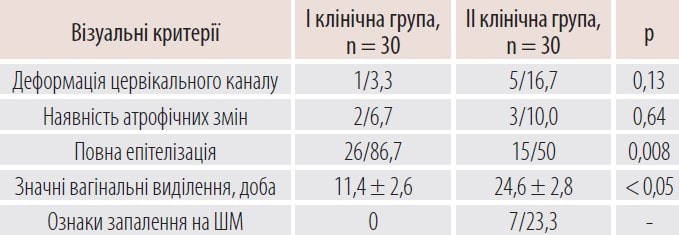
Водночас у пацієнток групи порівняння повна епітелізація через 1 місяць була діагностована в 15 (50,0%) випадках (відносний ризик (ВР) 0,27, 95% довірчий інтервал (ДІ) 0,10–0,71, р = 0,008). Зауважимо, що значні виділення у пацієнток основної клінічної групи статистично вірогідно тривали 11,4 ± 2,6 доби, що було менше, ніж у жінок групи порівняння – 24,6 ± 2,8 доби (р < 0,05). Ознаки атрофічних змін вагінального епітелію могли бути пов’язані з тим, що вказані пацієнтки перебували у клімактеричному періоді.
Під час аналізу результатів дослідження встановлено, що в групі порівняння процеси репарації були дещо сповільнені, у 7 жінок виявлені ознаки запалення ШМ, тоді як у пацієнток, які використовували розчин Декасан до виконання ексцизії ШМ та вагінальний гель Гінодек після хірургічного втручання, аналогічні ознаки не візуалізувалися.
Бактеріологічне дослідження, проведене через 3 місяці, виявило, що в більшості учасниць дослідження якісний склад вагінального вмісту відповідав показникам нормоценозу. У 27 (90,0%) пацієнток основної групи відзначався нормальний стан генітального біоценозу, при цьому подібний результат у групі порівняння був діагностований лише у 20 (66,7%) пацієнток (ВР 0,30, 95% ДІ 0,09–0,98, р = 0,047).
Аналіз вагінальної мікробіоти допоміг встановити зміни лактобацил через 3 місяці після оперативного лікування (табл. 2). У 26 (86,7%) пацієнток першої клінічної групи, які використовували вагінально препарат декаметоксину до та після хірургічного втручання, була достовірно більша кількість лактобацил у вагінальному секреті порівняно з 17 (56,7%) пацієнтками групи порівняння (ВР 0,31, 95% ДІ 0,11–0,84, р = 0,02).
Таблиця 2. Стан вагінального біоценозу у жінок з HSIL (ЦІН ІІ) залежно від комбінованої терапії через 3 місяці після ексцизії ШМ, абс. ч./%
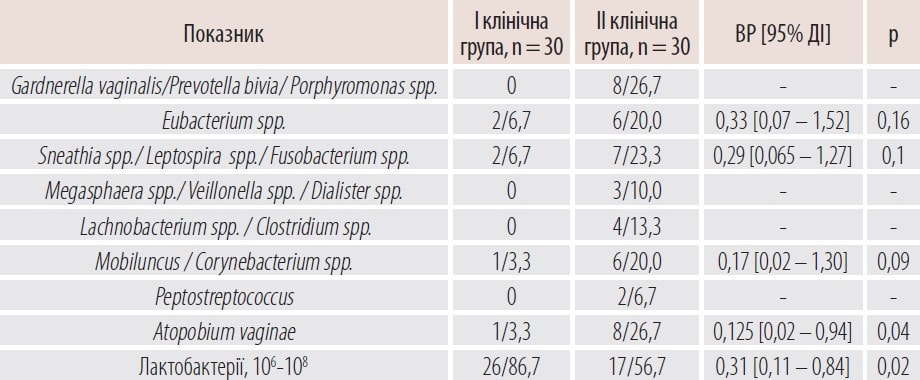
Через те, що молекули декаметоксину та лактобацили однаково позитивно заряджені, декаметоксин у складі розчину Декасан та гелю Гінодек толерантний до лактобацил, і йому може бути притаманна лактофлорозберігальна дія.
При дослідженні мікробіоценозу піхви також звертали увагу на кількісний склад умовно-патогенних мікроорганізмів у цервікальному слизі. Було відзначено, що внаслідок передопераційного використання розчину Декасан курсом 7 діб та післяопераційного застосування вагінального гелю Гінодек курсом 14 днів відбулося достовірне зниження показників анаеробної умовно-патогенної флори порівняно з 2 групою.
В основній групі через 3 місяці після ексцизії (конізації) ШМ була відсутня Gardnerella vaginalis та інші умовно-патогенні бактерії, тоді як у групі порівняння вказані мікроорганізми були виявлені у 8 пацієнток (26,7%). Кількість випадків діагностики Eubacterium spp. була меншою після лікування декаметоксином у жінок 1 групи в порівнянні з 2 (ВР 10,33, 95% ДІ 0,07–1,52, р = 0,16). Через 3 місяці від початку комбінованої терапії спостерігалось порівняно зменшення випадків діагностики комплексу Mobiluncus/Corynebacterium spp. у пацієнток із HSIL (ЦІН ІІ) 1 та 2 групи (ВР 0,17, 95% ДІ 0,02–1,30, р = 0,09). Також достовірно зменшилася кількість випадків виявлення Atopobium vaginae, ймовірно асоційованого з розвитком БВ, у пацієнток 1 групи (ВР 0,125, 95% ДІ 0,02–0,94, р = 0,04).
Через три місяці після оперативного лікування однією з особливостей репаративних процесів після комбінованої терапії HSIL (ЦІН ІІ), виявлених за допомогою кольпоскопії, була виражена васкуляризація епітеліальної поверхні. Нормальна кольпоскопічна картина (або повна епітелізація) характеризувалася наявністю багатошарового плоского епітелію на всіх зонах та квадрантах ШМ, епітеліальний стик збережений, строма звичайна, судини задовільно реагували на 3% розчин оцтової кислоти, проба Шиллера була позитивна.
Стосовно часу повної репарації післяопераційних ранових дефектів ШМ, то вона визначалася у термін 34,6 ± 4,1 та 42,4 ± 4,7 доби відповідно у пацієнток 1 та 2 групи дослідження. Загоєння операційної рани в жінок основної клінічної групи відбувалося на тлі формування ніжного струпа, без розвитку рубцевої деформації ШМ.
При проведенні цитологічного дослідження після трьох місяців від завершення терапії в обох групах відзначалося достовірне поліпшення якості цитологічної картини: зменшення кількості спостережень цитологічної картини третього класу та збільшення числа цитологічних змін, характерних для першого-другого класів.
Через 6 місяців після лікування спостерігалася більша кількість випадків нормальної кольпоскопічної картини в групах пацієнток, які отримували хірургічне лікування патології ШМ на тлі БВ. Результати контрольної кольпоскопії також свідчили про відсутність грубого рубцювання на ШМ у всіх клінічних групах.
Аномальна кольпоскопічна картина після лікування у вигляді слабкого ураження (LSIL) була діагностована у 2 (6,7%) пацієнток 2 групи. Інші кольпоскопічні картини, що мали ознаки запалення, спостерігали у 3 пацієнток цієї самої групи.
Через 6 місяців після лікування при контрольному цитологічному дослідженні було діагностовано відсутність інтраепітеліального ураження або малігнізації в 54 (90%) пацієнток, обстежених та пролікованих у нашому проспективному клінічному дослідженні (табл. 3).
Таблиця 3. Результати цитологічного дослідження у жінок з HSIL (ЦІН ІІ) через 6 місяців після комбінованої терапії
 * NILМ (Negative for Intraepithelial Lesion or Malignancy) – інтраепітеліальних змін або малігнізації не виявлено
* NILМ (Negative for Intraepithelial Lesion or Malignancy) – інтраепітеліальних змін або малігнізації не виявлено
**ASC-US (Аtypical Squamous Cells Undertermined Significance) – клітини плоского епітелію з атипією неясного значення
У першій групі з ЦІН цитологічний контроль на тлі проведеного лікування показав регрес HSIL зі 100,0% до 0,0%.
При контролі ВПЛ-статусу через 6 місяців після комбінованого лікування ВПЛ був виявлений у 2 (6,7%) жінок 1 групи та в 9 (30,0%) 2 групи (ВР 0,22, 95% ДІ 0,05–0,94, р = 0,04) (табл. 4). До того ж у пацієнток другої групи спостерігалося поєднання кількох типів ВПЛ високоонкогенного ризику.
Таблиця 4. Результати діагностики генотипів вірусу у ВПЛ-позитивних жінок із патологією ШМ після лікування
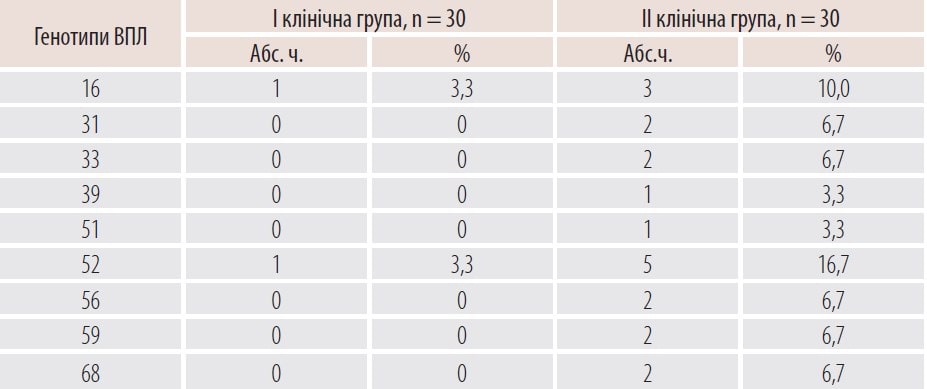
Не виявлено жодної побічної дії розчину Декасан та вагінального гелю Гінодек ані під час проведення терапії, ані в пізніші терміни.
На нашу думку, кращий терапевтичний ефект у комбінованому лікуванні HSIL на тлі БВ при використанні розчину Декасан та вагінального гелю Гінодек був пов’язаний із тим, що декаметоксин має антимікробну, протигрибкову дію, концентрується на цитоплазматичній мембрані мікробної клітини та з’єднується з фосфатидними групами ліпідів мембран, порушуючи проникність згаданої мембрани мікроорганізмів.
Гель Гінодек підтримує рН і вологість слизової піхви, завдяки чому усувається дискомфорт та сухість. Крім того, 0,5% гіалуронова кислота, яка входить до складу гелю Гінодек, покращує процеси репарації епітелію слизової оболонки ШМ, усуває сухість, зміцнює стінки піхви і підвищує їхню еластичність, завдяки чому поліпшується якість життя жінки.
Висновки
- Використання у складі комбінованої терапії HSIL (ЦІН ІІ) препаратів декаметоксину та гіалуронової кислоти призводило до більш швидкої та повноцінної епітелізації ранової поверхні, ніж використання стандартної терапії (ВР 0,27, 95% ДІ 0,10–0,71, р = 0,008).
- Через 3 місяці після вагінального застосування препаратів декаметоксину визначалося достовірне зростання частоти нормалізації вагінальної мікробіоти (ВР 0,30, 95% ДІ 0,09–0,98, р = 0,047), а також збільшення кількості лактобацил у вагінальному секреті (ВР 0,31, 95% ДІ 0,11–0,84,
р = 0,02). - Через 6 місяців після комбінованої терапії HSIL (ЦІН ІІ) встановлено статистично вірогідний вплив вагінального використання розчину декаметоксину та вагінального гелю з декаметоксином, гіалуроновою кислотою і лактатним буфером на сприяння елімінації онкогенних штамів ВПЛ (ВР 0,22, 95% ДІ 0,05–0,94, р = 0,04).
- Не було відзначено жодної побічної дії на організм жінки вагінального використання препаратів декаметоксину як під час терапії, так і на пізніших строках.
Конфлікт інтересів: автори заявляють, що досягли консенсусу та не мають конфлікту інтересів.
Автори:
• О.А. ТАРАН, д. мед. н., професор кафедри акушерства і гінекології №1 Вінницького НМУ ім. М.І. Пирогова, м. Вінниця
• В.О. РУДЬ, д. мед. н., професор кафедри акушерства і гінекології №2 Вінницького НМУ ім. М.І. Пирогова, м. Вінниця
• О.В. БУЛАВЕНКО, д. мед. н., професор, зав. кафедрою акушерства та гінекології №2 Вінницького НМУ ім. М.І. Пирогова, м. Вінниця
• Д.Г. КОНЬКОВ, д. мед. н., професор кафедри акушерства і гінекології №1 Вінницького НМУ ім. М.І. Пирогова, м. Вінниця
Література:
- Володько, Н.А. Український національний консенсус з обстеження та лікування жінок після проходження первинного цервікального скринінгу / Н.А. Володько, А.Б. Вінницька, В.В. Камінський [та ін.] // Репродуктивна ендокринологія. – 2018. – №5 (43). – С. 8–14.Volodko, N.A., Vinnytska, A.B., Kaminskyi, V.V., et al. “Ukrainian national consensus on the examination and treatment of women after primary cervical screening.” Reproductive Endocrinology 5.43 (2018): 8–14.
- Коньков, Д.Г.Клінічна ефективність вагінальних супозиторіїв, що містять мірамістин, у користувачів акушерського песарію при неспецифічному вагініті / Д.Г. Коньков, А.В. Старовєр, О. В. Булавенко, А. В. Вознюк // Здоровье женщины. – 2017. – №7. – С. 2–7.Konkov, D.G., Starover, A.V., Bulavenko, O.V., Vozniuk, A.V. “The clinical efficiency of vaginal suppositories containing miramistin, for pregnant women with nonspecific vaginitis before installation of cervical pessaries.” Woman’s Health 7 (2017): 2–7.
- Коньков, Д.Г. Особливості клінічного застосування пробіотиків в акушерській практиці / Д.Г. Коньков // Здоровье женщины. – 2020. – № 3. – С. 42–47.Konkov, D.G. “The features of clinical applying of probiotics in obstetric practice.” Woman’s health 3 (2020): 42–7.
- Коньков, Д.Г. Особливості комплексної терапії бактеріального вагінозу у вагітних із порушенням затульної функції шийки матки / Д.Г. Коньков, Н.В. Адамчук, В.В. Кливак // Репродуктивна ендокринологія. – 2020. – №4 (54). – С. 59–65.Konkov, D.G., Adamchuk, N.V., Klivak, V.V. “The features of complex therapy of bacterial vaginosis in pregnant women with cervical incompetence.” Reproductive endocrinology 4.54 (2020): 59–65.
- Таран, О.А.Клінічний досвід в оптимізації репаративних процесів шийки матки після деструктивно-хірургічних втручань / О.А. Таран, О.В. Булавенко, Д.Г. Коньков, Т.В. Лобастова // Здоровье женщины. – 2019. – №3 (139). – С. 38–42.Taran, O.А., Bulavenko, O.V., Konkov, D.G., Lobastova, T.V. “Clinical advice in the optimization of the reparative processes of the uterine cervix due to destructive surgical involvement.” Woman’s health 3.139 (2019): 38–42.
- Таран, О.А. Сучасний погляд на оптимальну терапію ВПЛ-асоційованої патології шийки матки на тлі вагінального дисбіозу / О.А. Таран, О.В. Булавенко, Д.Г. Коньков, Т. В. Лобастова // Репродуктивна ендокринологія. – 2018. – №6 (44). – С. 16–20.Taran, O.А., Bulavenko, O.V., Konkov, D.G., Lobastova, T.V. “The modern view on optimal therapy of HPV-associated pathology of cervix at the vaginal dysbiosis background’s.” Reproductive endocrinology 6.44 (2018): 16–20.
- Aitken, C.A., Siebers, A.G., Matthijsse, S.M., et al. “Management and treatment of cervical intraepithelial neoplasia in the Netherlands after referral for colposcopy.” Acta Obstet Gynecol Scand 98.6 (2019): 737–46.
- Chao, Y.S., McCormack, S. HPV Self-sampling for primary cervical cancer screening: a review of diagnostic test accuracy and clinical evidence – An Update. Ottawa (ON). Canadian Agency for Drugs and Technologies in Health (2019).
- Champer, M., Wong, A.M., Champer, J., et al. “The role of the vaginal microbiome in gynaecological cancer.” BJOG 125.3 (2018): 309–15.
- Chehoud, C., Stieh, D.J., Bailey, A.G., et al. “Associations of the vaginal microbiota with HIV infection, bacterial vaginosis, and demographic factors.” AIDS 31.7 (2017): 895–904.
- Demarco, M., Egemen, D., Raine-Bennett, T.R., et al. “A study of partial human papillomavirus genotyping in support of the 2019 ASCCP Risk-Based Management Consensus Guidelines.” Journal of Lower Genital Tract Disease 24.2 (2020): 144–7.
- Jansen, E.E.L., Zielonke, N., Gini, A., et al. “Effect of organised cervical cancer screening on cervical cancer mortality in Europe: a systematic review.” European Journal of Cancer 27 (2020): 207–23.
- Gilham, C., Sargent, A., Kitchener, H., Peto, J. “HPV testing compared with routine cytology in cervical screening: long-term follow-up of ARTISTIC RCT.” Health Technol Assess 23 (2019).
- Liang, Y., Chen, M., Qin, L., et al. “A meta-analysis of the relationship between vaginal microecology, human papillomavirus infection and cervical intraepithelial neoplasia.” Infect Agent Cancer 14 (2019): 29.
- Perkins, R.B., Guido, R.S., Castle, P.E., et al. “ASCCP risk-based management consensus guidelines for abnormal cervical cancer screening tests and cancer precursors. 2019 ASCCP Risk-Based Management Consensus Guidelines Committee.” J Low Genit Tract Dis 24 (2020): 102–31.
- Sodhani, P., Gupta, S., Gupta, R., Mehrotra, R. Bacterial vaginosis and cervical intraepithelial neoplasia: is there an association or is co-existence incidental?. Asian Pac J Cancer Prev. 2017; 18(5): 1289-1292.
- Taran, O., Konkov, D., Lobastova, T. “The criteria for prognostic monitoring of cervical neoplasia.” The proceedings of the 27th biannual European Congress of Obstetrics and Gynaecology EBCOG. Bergen, Norway (2020).
- World Health Organization. Introducing and scaling up testing for human papillomavirus as part of a comprehensive programme for prevention and control of cervical cancer: a step-by-step guide. Geneva. WHO (2020).