Возможности коррекции синдрома гемореологической недостаточности в интенсивной терапии больных с острым панкреатитом
Днепропетровская государственная медицинская академия, кафедра анестезиологии, интенсивной терапии и медицины неотложных состояний ФПО
Украина, г. Днепропетровск, ул.Дзержинского, 9
Резюме: В статье представлены результаты оценки эффективности применения нового украинского инфузионного препарата Латрен для коррекции синдрома гемореологической недостаточности у больных с острым панкреатитом.
Ключевые слова: острый панкреатит, синдром гемореологической недостаточности, микроциркуляция, пентоксифиллин, Латрен
Проблема интенсивной терапии острого панкреатита (ОП) — одна из наиболее сложных и актуальных. В последнее десятилетие отмечается неуклонный рост частоты острого панкреатита в структуре хирургической патологии органов брюшной полости. Благодаря современным методам диагностики, лечения и профилактики летальность при ОП в последние годы снизилась до 6-21%, однако, при деструктивных формах ОП эта цифра стабильно составляет 50-85%, а среди выживших больных — у 73% возникает стойкая утрата трудоспособности, что придает данной проблеме неоспоримую социальную значимость, поскольку пик заболеваемости приходится на лиц активного трудоспособного возраста 30-50 лет [4]. Панкреонекроз, имевший в начале нашего века славу одной из наиболее внушительных катастроф в брюшной полости, до настоящего времени остается заболеванием с непрогнозируемым исходом. Эндогенная интоксикация и расстройства микрогемодинамики являются ключевыми звеньями патогенеза при деструктивных формах ОП, определяют тяжесть течения и прогноз заболевания. Токсическое воздействие на организм оказывают активизированные панкреатические и лизосомальные ферменты, калликреин-кининовая система, биогенные амины, пептиды средней молекулярной массы, активация ПОЛ. Одним из уровней реализации патологических эффектов панкреатогенной токсемии являются генерализованные макро- и микроциркуляторные нарушения, которые лежат в основе развития синдрома полиорганной недостаточности при ОП. Гемодинамические нарушения появляются на ранних стадиях и сопровождают все периоды заболевания. Наиболее же глубокие изменения при остром панкреатите происходят на уровне микроциркуляторного русла. Они характеризуются замедлением линейной скорости кровотока, агрегацией и стазом форменных элементов крови, повышением проницаемости сосудов – то есть развитием синдрома гемореологической недостаточности. Данный синдром развивается при ряде других заболеваний общехирургического генеза. По литературным данным установлено, что на фоне тяжелой интоксикации и выраженных микроциркуляторных нарушениях происходят значительные изменения свойств форменных элементов крови. Высокая адгезивно-агрегационная способность лейкоцитов и тромбоцитов провоцирует нарушение целостности эндотелиального слоя, инициирует возникновение внутрисосудистых изменений, активизирует процесс свертывания крови и способствует микро — и макротромбообразованию. Все это способствует снижению тканевой перфузии, а при вовлечении в процесс значительных сосудистых бассейнов появляются прямые предпосылки формирования полиорганной недостаточности [6]. Своевременная и адекватная коррекция адгезивно-агрегационных нарушений форменных элементов крови, реологического состояния плазмы позволит нормализовать взаимоотношения сосудистого эндотелия с тромбоцитами и лейкоцитами. Общепризнанным элементом патогенетической терапии острого панкреатита является необходимость коррекции синдрома гемореологической недостаточности.Пока основным способом коррекции гемореологии остается медикаментозная терапия.
Среди средств, достоверно улучшающих реологические свойства крови и микроциркуляцию, наиболее изученным и эффективным препаратом является пентоксифиллин. Пентоксифиллин является производным метилксантина и по химической структуре близок к теобромину, эуфиллину и теофиллину [2, 3]. Под влиянием пентоксифиллина достоверно увеличивается деформируемость, эритроцитов, уменьшается их агрегационная активность и улучшается текучесть крови [8]. Влияя на взаимодействие между гранулоцитами, тромбоцитами, эритроцитами и эндотелием, пентоксифиллин также улучшает реологические свойства крови в системе микроциркуляции и увеличивает способность отдавать кислород тканям в зоне ишемии. Кроме того, под действием пентоксифиллина наблюдается не только расширение, но и увеличение количества функционирующих капилляров, ускорение капиллярного кровотока, уменьшение количества участков накопления форменных элементов крови, увеличивается транскапиллярный обмен и микролимфоток [3, 2, 7]. Эти доказанные свойства пентоксифиллина обуславливают потенциальную способность препарата влиять на реологические характеристики крови. Пентоксифиллин оказывает регулирующее влияние на свертываемость крови за счет ряда эффектов: угнетение вазоконстрикции в микроциркуляторном русле, способствование уменьшению уровня фибриногена и тромбина плазмы, стимуляция фибринолиза, повышение концентрации активатора тканевого плазминогена. Не менее важным признается воздействие пентоксифиллина на лейкоциты, особенно гранулоциты, и опосредованный этим иммуномодулирующий эффект препарата. Показано, что пентоксифиллин увеличивает деформируемость нейтрофилов и уменьшает их активность что, свою очередь, обусловливает уменьшение образования свободных радикалов, их адгезии и агрегации, освобождение элластазы, уменьшение уровней воспалительных цитокинов в крови, а также увеличивает деформируемость моноцитов [1, 3, 4]. Есть данные, что кроме основной функции лейкоцитов – антимикробной, при воспалительных процессах, большое значение имеет их влияние на кровоток. Обнаружена связь между состоянием лейкоцитов, уровнем вязкости цельной крови и микроциркуляторной перфузией. Пентоксифиллин также блокирует действие воспалительных цитокинов, которые регулируют функцию клеток сосудистой стенки. Эффекты данного препарата на эритроциты и нейтрофилы частично связаны с ингибированием фосфодиэстеразы и последовательным увеличением внутриклеточной цАМФ, которая играет роль в контроле активации и пролиферации моноцитов, макрофагов, Т- и В-лимфоцитов.
На сегодняшний день компания «Юрия-Фарм» начала производство нового лекарственного препарата – Латрен. Латрен – это раствор для инфузий, в котором сбалансированный изоосмолярный раствор электролитов (Рингер-лактатный) потенцирует действие пентоксифиллина. Важно также то, что это готовая лекарственная форма, произведенная промышленным способом, исключающим технические ошибки и возможность инфицирования раствора при приготовлении ex tempore. Препарат интересен тем, что, обладая свойствами пентоксифиллина, оказывает более выраженное действие на микроциркуляцию благодаря наличию сбалансированного раствора электролитов, который дополнительно улучшает реологические свойства крови и нормализует электролитный состав плазмы.
Таким образом, цель настоящего исследования – изучить эффективность препарата Латрен для коррекции синдрома гемореологической недостаточности при проведении интенсивной терапии больных с острым панкреатитом.
Материал и методы.
В исследовании приняли участие 20 пациентов с острым панкреатитом в возрасте от 20 до 75 лет. Больные поступили в отделение анестезиологии и интенсивной терапии клинической больницы №6 г. Днепропетровска для проведения интенсивной терапии и принятия решения о необходимости хирургического вмешательства. На фоне полного комплекса интенсивной терапии острого панкреатита для коррекции микроциркуляторных расстройств больным назначался Латрен внутривенно по 200 мл 2 раза в сутки.
Клинико-лабораторное обследование было поэтапным: 1 этап – состояние при госпитализации; 2 этап – до введения Латрена; 3 этап – через 12 час после инфузии Латрена.
Для определения степени тяжести дегидратации и объема растворов для корригирующей инфузионной терапии использовали пробу на гидрофильность тканей по П.И. Шелестюку, которая соответствовала определенной степени дегидратации. Для определения степени микроциркуляторных нарушений использовали пробу «белого пятна», проводился обязательный учет диуреза.
Для оценки состояния больных и эффективности реологической терапии использован комплекс методов исследования: динамическая регистрация показателей кровообращения (АД, ЧСС, ЦВД, ЭКГ), кислотно-щелочного состояния, гематологических показателей (Нb, Ht, тромбоциты); пульсовая оксиметрия, коагулограмма (активированное частичное тромбопластиновое время — АЧТВ, тромбиновое время — ТВ, протромбиновое время — ПВ, АДФ-индуцированная агрегация тромбоцитов, содержание фибриногена (Ф), продуктов деградации фибрина (ПДФ) и растворимых фибрин-мономерных комплексов (РФМК) в плазме крови, фибринолиз-тест), показатели вискозиметрии (вязкость цельной крови — ВЦК, индекс агрегации эритроцитов, индекс деформации эритроцитов). Определение фактора Виллебранда производилась по материалам инструкции к набору агрегометра 220LA. Спонтанная агрегатометрия тромбоцитов проводилась по методике Born. , уровень адгезии лейкоцитов определялся по Mc Gregory.
Учитывая тяжесть состояния, необходимость проведения длительной и объемной инфузионной терапии, динамического контроля биохимических показателей крови и центрального венозного давления (ЦВД), больным проводилась катетеризация центральной подключичной вены справа. Все больные, поступающие в отделение анестезиологии и интенсивной терапии, получали основной комплекс мероприятий, включающий: восстановление дефицита объема циркулирующей крови солевыми растворами, восстановление центральной и периферической гемодинамики, улучшение реологических свойств крови, нормализацию функции дыхания, стабилизацию клеточных мембран, коррекцию кислотно-щелочного и водно-электролитного состояния. Бессолевые растворы не использовались. В зависимости от степени тяжести гиповолемии объем проводимой инфузионно-трансфузионной терапии составлял от 80 до 110 мл/кг сутки.
Анализ результатов проведен с помощью статистической обработки с вычислением парных корреляций, оценкой достоверности отличий по критерию Стьюдента. При обработке данных использовали программный продукт Microsoft Excel.
Результаты и их обсуждение.
Особый интерес представляет возможности коррекции гемокоагуляции и реологии с первых часов госпитализации больного. При поступлении в ОИТ у всех больных имелись признаки повышенной тромбоопасности: снижение фибринолитической активности, увеличение вязкости цельной крови, плазмы и сыворотки, РМФК, агрегационной тромбоцитов и эритроцитов.
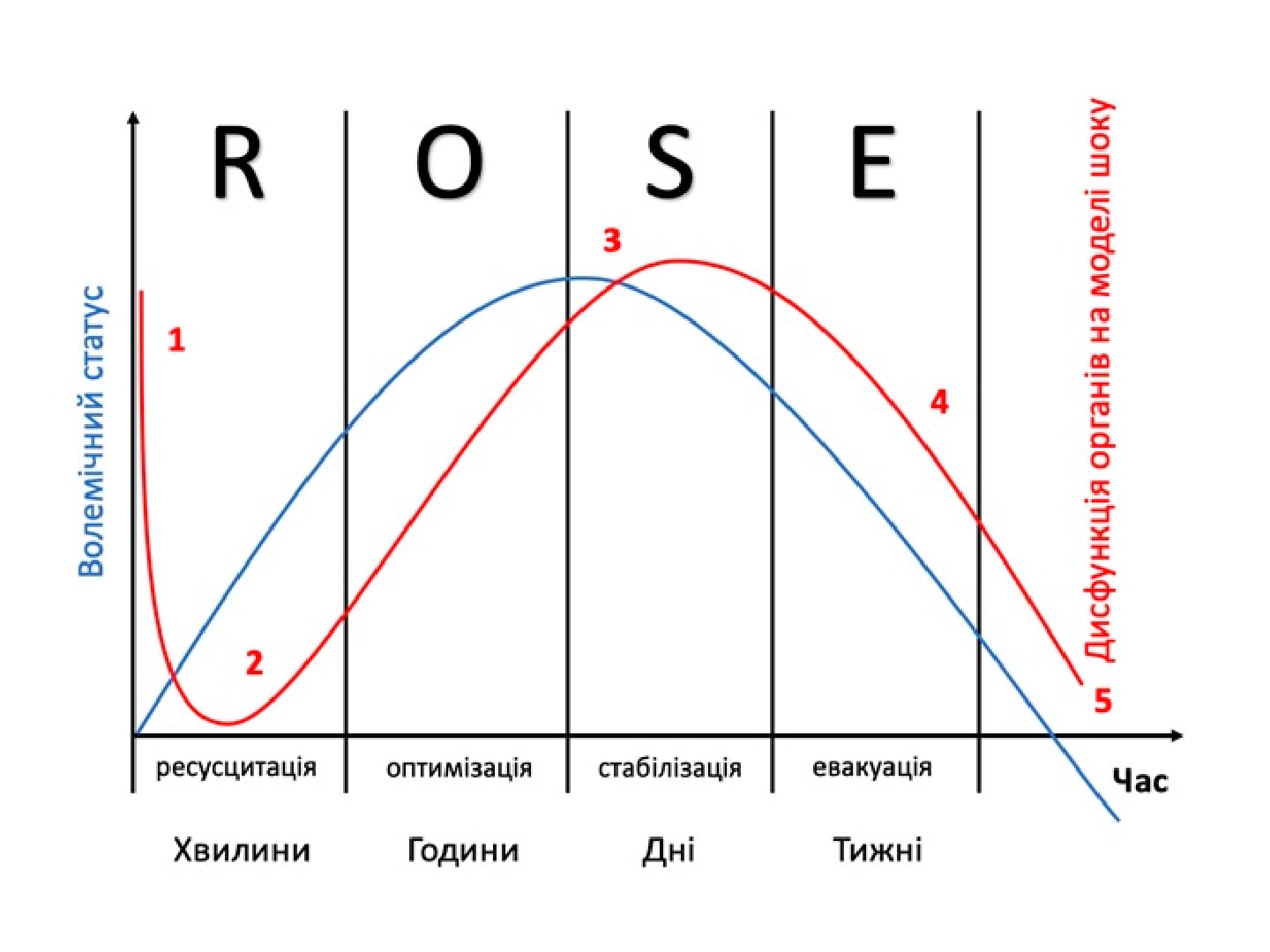
Проведение инфузионной терапии в условиях шокового состояния больного считается определяющим фактором не только стабилизации гемодинамики, но и оптимизации периферического кровотока. Ввиду проводимой гемодилюции мы наблюдали снижение значений гемоглобина и гематокрита. Исходный средний уровень Нb составил 163,8 ± 4,5 г/л, Нt — 48,8 ± 1,6 %. Через 12 часов после начала интенсивной терапии эти показатели снижались до 116,1 ± 5,8 г/л и 34,7 ± 1,8 %, что соответствовало оптимальным реологическим условиям.
Динамика показателей свертывания крови характеризовалась сохранением в пределах нормальных значений времени начала свертывания при наличии тенденции к увеличению времени окончания и общей продолжительности свертывания , т. е. происходило замедление образования сгустка, что в сочетании с поддержанием хорошей периферической циркуляции является положительным фактором профилактики тромбообразования.
Содержание тромбоцитов коррелировало с проведением гемодилюции, снижаясь по сравнению с исходным, но не опускаясь ниже нормы.
Показатели коагуляционного звена свертывающей системы крови (АЧТВ, ПВ, ТВ) на всех этапах исследования оставались в пределах нормальных значений.
Фибринолитическая активность, содержание растворимых фибрин-мономерных комплексов и продуктов деградации фибрина на этапах исследования изменялись незначительно, причем исходно фибринолитическая активность была снижена, а содержание растворимых фибрин-мономерных комплексов повышено, что типично для больных с тяжелым течением острого панкреатита.
Для подтверждения выбора метода коррекции гиперагрегации у больных с синдромом гемореологической недостаточности целесообразно исследовать функциональную активность тромбоцитов и лейкоцитов в результате воздействия на них фармакологического препарата. С этой целью мы исследовали влияние Латрена на состояние агрегации тромбоцитов и лейкоцитов in vitro.
При анализе изменения агрегационных свойств тромбоцитов и лейкоцитов in vitro в результате применения Латрена мы получили следующие данные: уровень спонтанной агрегации снизился с 10,9±2,7 % до 2,5±0,78 % (р<0,01), что составило соответственно 77,1%. Изменение лейкоцитарной адгезии происходило по аналогичной схеме: снижение функциональной активности лейкоцитов произошло с 32,7±4,1% до 26,4±3,5%, соответственно на 19,3%.
При дальнейшем исследовании мы обратили внимание на факторы, инициирующие агрегацию и адгезию. Фибриноген в исследуемой группе снизился на 6% (с 459±20 до 431±28 мг%), фактор Виллебранда на 8% ( со 190±22 до 175±12 %). Общая вязкость крови у больных на 1 и 2 этапах составляла 6,3±0,8 и 6,2±0,7 сПуаз, но на 3 этапе снизилась до 5,5±1,3, что составило 12 %. Вязкость плазмы у больных с острым панкреатитом на фоне применения Латрена уменьшилась на 16% (с 3,2±0,6 до 2,7±0,5 сПуаз).
Снижение уровня факторов агрегации в плазме закономерно привело к изменению активности лейкоцитов и тромбоцитов. Так, спонтанная агрегация тромбоцитов снизилась на этапах исследования с 13,2±0,9 до 8,2±1,1%, а степень адгезии лейкоцитов – с 45±3,8 до 40±5,1%.
Любое лечение больных с проявлениями гемореологической недостаточности имеет целью улучшение метаболизма за счет повышения эффективной доставки субстратов окисления и кислорода, в зону регионарной ишемии. Поэтому в исследовании мы также проводили оценку критерия результативности реологической терапии в свете кислородного баланса и изменения кислотно-щелочного состояния. Так, компенсированный метаболический ацидоз у больных при поступлении на этапах терапии нормализовался, что свидетельствовало о снижении явлений гемореологических расстройств и улучшении состояния микроциркуляции под влиянием Латрена.
Выводы:
- У больных с острым панкреатитом при поступлении выявляются маркеры повышенной тромбоопасности: снижение фибринолитической активности, увеличение вязкости цельной крови, плазмы и сыворотки, РМФК.
- Адекватная инфузионная терапия позволяет провести коррекцию гемоконцентрации и привести уровни гемоглобина, гематокрита и тромбоцитов к оптимальным реологическим соответствиям.
- Применение Латрена позволяет в значительной степени купировать проявление синдрома гемореологической недостаточности в виде снижения факторов агрегации, оптимизации уровней спонтанной агрегации тромбоцитов и степени адгезии лейкоцитов.
- Полученные данные позволяют рекомендовать Латрен для коррекции микроциркуляторных расстройств у больных с острым панкреатитом.