Ефективність застосування моксифлоксацину у лікуванні позагоспітальної пневмонії
В оглядовій статті приведені результати вітчизняних та міжнародних досліджень використання фторхінолону 4-го покоління Моксифлоксацину у лікуванні позагоспітальної пневмонії та пневмонії спричиненої SARS-CoV-2. Аналіз клінічного застосування препарату моксифлоксацин в лікуванні інфекційних ускладнень респіраторних шляхів свідчить про його високу ефективність та біодоступність, низький ризик формування резистентності, що дозволяє рекомендувати його для широкого використання в роботі практикуючого лікаря. А генерик Максіцин ( Юрія-фарм), який випускається у вигляді концентрата 20 мг / мл у флаконі 20 мл, дозволяє значно знизити вартість лікування та оптимізувати інфузійну терапію шляхом вибору і об’єму і розчинника.
Ключові слова: фторхінолони, моксифлоксацин, лікування, пневмонія, COVID-19.
Позалікарняна пневмонія (ПП) є однією з найпоширеніших інфекційних хвороб у всьому світі [ 1 ]. Зафіксовані випадки захворюваності на ПП у різних країнах коливаються від 1,6 до 11 на 1000 дорослих, хоча точні дані важко встановити, оскільки не існує універсального визначення для діагностики ПП[ 2 ].
ПП є основною причиною захворюваності, госпіталізації, смертності та погіршення якості життя, і пов’язаний із значним соціальним навантаженням на охорону здоров’я. У країнах Західної Європи рівень госпіталізації хворих на ПП коливається приблизно від 10% до 60%, в основному залежно від групи пацієнтів, яких досліджують [ 3,4 ]. Рівень смертності від ПП коливається від <5% у амбулаторних пацієнтів до 10% у пацієнтів, що госпіталізовані та перевищує 30% у реанімаційних пацієнтів [ 5 ]. Частота захворюваності на ПП та смертність, пов’язану з ПП, різко зростає з віком і помітно вище у чоловіків, ніж у жінок [ 4 , 6 ].
Основними збудниками ПП є Streptococcus pneumoniae, Haemophilus influenzae та Moraxella catarrhalis , які разом становлять приблизно 85% випадків [ 7 ]. До «атипових» збудників інфекційних захворювань належать Mycoplasma pneumoniae , Chlamydophila pneumoniae та Legionella pneumophila. У багатьох хворих на ПП є змішані інфекції, що включають як типові, так і атипові патогени [ 8,9 ].
На сьогоднішній день ще одним агресивним збудникиком, який призводить до важкої ускладненої позагоспітальної пневмонії є вірус SARS-COV-2.
Поява коронавірусу SARS-CoV-2 викликала безпрецедентну загрозу у всьому світі. Ще з початку пандемії, дослідники та клініцисти зосередилися на перепрофілюванні існуючих антибіотиків, противірусних та протизапальних препаратів, щоб знайти ефективну терапію для боротьби COVID-19.
Фторхінолони, сімейство 6-фтор-7-піперазиніл-4-хінолони, є синтетичними протимікробними засобами широкого спектру дії, отримані з хінолонів з додаванням атома фтору, приєднаного до центрального кільця [10]. Вони володіють бактерицидним ефектом в результаті впливу на бактеріальну ДНК-гіразу (топоізомераза типу II) та топоізомераза IV, таким чином, інгібуючи синтез бактеріальної ДНК і приводячи до розщеплення бактеріальної ДНК та швидкої загибелі бактерій [11]. Фторхінолони активні щодо грамнегативних та грампозитивних бактерій, анаеробів, мікобактерій та атипових збудників.
Згідно нових досліджень зарубіжних вчених стало відомо, що фторхінолони володіють противірусною дією проти вірусу коров’ячої віспи, паповавірусу, CMV, VZV, HSV-1, ВПГ-2, ВІЛ. У механізмі дії фторхінолонів (ципрофлоксацин і моксифлоксацин) лежить пригнічення реплікації SARS-CoV-2, виявляючи більш сильну здатність зв’язуватися з його основною протеазою, ніж хлорохін і нелфінавір ( антиретровірусних препаратів, інгібіторів протеази). Примітно, що фторхінолони продемонстрували множинну імуномодулюючу дію, що веде до ослаблення запальної реакції через інгібування прозапальних цитокінів.
Слід зазначити, що респіраторні фторхінолони, такі як левофлоксацин та моксифлоксацин є терапевтичними агентами першої лінії для лікування важкої позалікарняної пневмонії. Вони характеризуються вигідними фармакокінетичними властивостями; більш високими концентраціями в легенях; і відмінним профілем безпеки порівняно з іншими антибіотиками, що використовуються для лікування респіраторних інфекцій, такими як макроліди і бета-лактами [10].
Характеристика моксифлоксацину
Моксифлоксацин, як і інші нові фторхінолони, має широкий антибактеріальний спектр, що забезпечує прекрасне перекриття основних збудників, що вражають дихальні шляхи. Він проявляє чудову активність щодо грамнегативних паличок (Enterobacteriaceae, H. influenzae , M. catarrhalis ) та покращує грампозитивну активність щодо S.pneumoniae (як пеніциліночутливих, так і пеніцилінорезистентних штамів), а також S. aureus у порівнянні з ципрофлоксацином. Більш того, він зберігає хорошу активність щодо атипових збудників із значно кращим антибактеріальним ефектом проти Legionella pneumophila порівняно з еритроміцином і демонструє покращену активність щодо анеробів порівняно з ципрофлоксацином [12].
Моксифлоксацин може інгібувати як ДНК -гіразу, так і топоізомеразу IV, але механізм його дії дещо відрізняється від механізму дії інших фторхінолонів. Для S. pneumoniae переважна ціль дії фторхінолонів, схоже, змінюється залежно від обраного антибактеріального засобу.
Моксифлоксацин насамперед націлений на субодиницю gyrA ДНК -гірази, тоді як левофлоксацин та інші менш сучасні похідні, такі як офлоксацин та ципрофлоксацин, переважно націлюються на субодиниці parC або parE топоізомерази IV. Завдяки цій різниці моксифлоксацин може зберігати високу активність проти все більш поширених штамів пневмококів, що несуть заміни в топоізомеразі IV через широке використання старих похідних. Крім того, у зв’язку з модифікацією в положенні С-7 структури фторхінолонів, моксифлоксацин є перешкоджаючим чинником для S. pneumoniae [13,14].
Моксифлоксацин можна вводити у вигляді пероральних та/або внутрішньовенних препаратів з чудовою біодоступністю; препарат добре всмоктується після перорального введення і досягає хорошого проникнення в тканини на рівні дихання, досягаючи вищих концентрацій в альвеолярних макрофагах (56,7 мкг/мл) та рідині епітеліальної оболонки (20,7 мкг/мл), ніж у сироватці крові (3,2 мкг/мл) після разової пероральної дози 400 мг [15]. Останнім часом високі внутрішньолегеневі концентрації також були підтверджені у літніх людей [16]. Крім того, моксифлоксацин як внутрішньовенно, так і перорально демонструє високе проникнення в легеневу тканину з максимальною концентрацією в легенях 12,37 мкг/г та 16,21 мкг/г для внутрішньовенного та перорального введення відповідно [17].
Моксифлоксацин метаболізується переважно за допомогою печінкових реакцій ІІ фази, активність яких, як було показано, не знижується з віком [18]. Коригування дози не є необхідним у пацієнтів похилого віку або у пацієнтів з нирковою або печінковою недостатністю легкого та помірного ступеня [19].
Профіль безпеки моксифлоксацину відповідає встановленому групі фторхінолонів. Реакції з боку шлунково-кишкового тракту – це найпоширеніший побічний ефект під час терапії. Як і інші фторхінолони, моксифлоксацин може спричинити подовження інтервалу QT; тому його слід уникати у пацієнтів з вже відомим подовженням інтервалу QT; пацієнтам з некоригованою гіпокаліємією або гіпомагніємією, а також у пацієнтів, які отримують антиаритмічні засоби класу IA (наприклад, хінідин, прокаїнамід) або класу III (наприклад, аміодарон, соталол) або з іншими препаратами, такими як деякі протимікробні засоби (наприклад, еритроміцин, галофантрин, пентамідин), деякими антигістамінними засобами (наприклад, астемізол, мізоластин, терфенадин), нейролептиками та трициклічними антидепресантами [20].
Моксифлоксацин має низьку схильність викликати фототоксичні реакції та низький потенціал викликати збуджуючі ефекти, і, як і інші агенти групи, потенційно може спричинити розлади сухожиль переважно у пацієнтів літнього віку за наявності одночасного застосування кортикостероїдів та хронічних захворювань нирок [19]
Моксифлоксацин не має інших значних лікарських взаємодій з низкою загальнопризначених препаратів, хоча його всмоктування зменшується при одночасному застосуванні заліза та катіонних антацидів [21].
Порівняльна ефективність моксифлоксацину у лікуванні позагоспітальної пневмонії
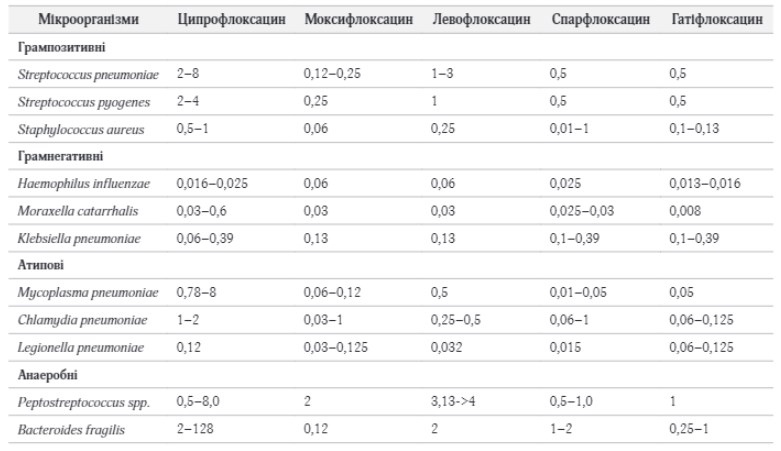
Серед препаратів останнього покоління фторхінолонів найбільшою активністю проти грампозитивних бактерій (пневмококів і стафілококів) має моксифлоксацин (табл. 1). Моксифлоксацин явно перевершує ципрофлоксацин та інші ранні фторхінолони за дією на пневмококи, стрептококи, стафілококи, хламідії і анаероби і не поступається за активністю на грамнегативні бактерії. Левофлоксацин поступається моксифлоксацину по активності на грампозитивні бактерії і анаероби.
Активність гатіфлоксацину та спарфлоксацина практично не відрізняється від активності моксифлоксацину, проте останній істотно перевершує перші два по фармакодинамічним показникам щодо S.pneumoniae [23]. Крім того, в даний час гатіфлоксацин і спарфлоксацин доступні тільки в пероральній формі, до того ж токсичність спарфлоксацина обмежує його широке застосування в медицині.
Таблиця 1. Активність фторхінолонів in vitro (МПК90, мг/л) по відношенню до позалікарняних штамів респіраторних патогенів
У дослідженні R.Finch з співавт. [24] клінічна ефективність моксифлоксацину в режимі монотерапії (внутрішньовенно 400 мг на добу, потім всередину 400 мг на добу) була вищою в порівнянні з комбінованою терапією амоксицилін / клавуланату і кларитроміцином – 93 і 85% відповідно. Бактеріологічна ефективність моксифлоксацину також була вище. Практично важливо, що терміни одужання пацієнтів при застосуванні моксифлоксацину були коротше. Фармако-економічний аналіз показав перевагу моксифлоксацину порівняно з комбінованою терапією: загальні витрати на лікування 1 випадку важкої пневмонії моксифлоксацином були менше на 266 Євро в Німеччині і 381 Євро у Франції [25].
Німецькі дослідники порівняли бактеріологічну активність левофлоксацину 500 мг та моксифлоксацину 400 мг проти клінічних збудників Staphylococcus aureus, Staphylococcus epidermidis, Escherichia coli, Klebsiella pneumoniae. Результати дослідження показали, що моксифлоксацин мав дуже хорошу бактерицидну активність щодо чутливих до хінолонів штамів чотирьох випробуваних видів бактерій. Моксифлоксацин досяг помітно кращої активності проти S. aureus та S. epidermidis у порівнянні з левофлоксацином [26].
У наукових даних вітчизняних та зарубіжних дослідників наведені клінічні дані застосування моксифлоксацину в режимі монотерапії при лікуванні важкої пневмонії. Також є вагомі аргументи на користь призначення моксифлоксацину при лікуванні ускладненої пневмонії (абсцедування, емпієма плеври) на підставі високої активності препарату in vitro проти найбільш важливих збудників – S.aureus, K.pneumoniae, анаеробів. Однак останні припущення вимагає підтвердження в контрольованих клінічних дослідженнях [23].
Велике проспективне дослідження було проведене у 12 країнах (Хорватія, Франція, Угорщина, Казахстан, Йорданія, Киргизстан, Ліван, Республіка Молдова, Румунія, Росія, Україна та Македонія) у 2014 році [27]. Проводили лікування людей > 18 років моксифлоксацином 400 мг на добу після госпіталізації з діагнозом позагоспітальна пневмонія. Всього у дослідження прийняло участь 2733 пацієнтів. Моксифлоксацин у дозі 400 мг один раз на день у середньому 10,0 днів (діапазон 2,0–39,0 днів) був високоефективним у лікуванні пацієнтів із ПП.
Повідомлялося про покращення у цілому ряді діагностичних показників, що регулярно моніторились в клінічній практиці, включаючи загальний стан пацієнта, тяжкість інфекції, симптоми задишки, кашлю, мокротиння, біль у грудному відділі та патологічні шуми при аускультації, температурна реакція і рентгенографія грудної клітки. Загалом 96,7% пацієнтів відчули поліпшення, тобто почувалися краще під час дослідження в середньому через 2,7 дня, і понад 94% пацієнтів відчули поліпшення через 5 днів.
Відмінностей у ефективності прийому моксифлоксацину не спостерігалася між пацієнти, які отримували моксифлоксацин шляхом внутрішньовенного введення самостійно або шляхом послідовного внутрішньовенного, а потім перорального введення. Також не було виявлено жодних відмінностей у ефективності моксифлоксацину між пацієнтами, які мали ускладнену пневмонію на початковому етапі.
Крім того, в останні роки чутливість типових збудників хвороб до пеніцилінів, макролідів та цефалоспоринів другого покоління знизилося, так що мультирезистентні штами, які викликають ПП набувають все більшого клінічного значення [27]. Незважаючи на цю тенденцію, моксифлоксацин був ефективним у великої частки пацієнтів у цьому дослідженні [27].
У 2007 році Товариство інфекційних хвороб Америки та Американське торакальне товариство опублікували нові вказівки щодо лікування дорослих пацієнтів із позалікарняною пневмонією [30]. У цих керівних принципах повідомлялося, що левофлоксацин, геміфлоксацин та моксифлоксацин однаково ефективні, як комбінація β-лактаму та макроліду, і були запропоновані як кращий варіант лікування для пацієнтів, які потребують госпіталізації, а також для пацієнтів із супутніми захворюваннями які лікуються амбулаторно.
Ефективність моксифлоксацину у лікуванні пневмоніі спричиненої SARS-CoV-2
На даний час немає спеціальних ліків або засобів лікування хвороб, викликаних SARS-CoV-2 (2019-nCoV). Пошук нових застосувань для вже затверджених препаратів з добре відомими фармакокінетичними характеристиками та профілем безпеки є більш економічним, а також набагато швидшим, ніж розробка нового препарату, і може складатися з ефективної стратегії терапії для подолання хвороб.
Так, згідно даних польських науковців фторхінолони крім своєї антибактеріальної активності володіють противірусною активністю. Вони мають сильну здатність зв’язуватися з основною протеазою COVID-19 (M pro ) [28]. Для цього дослідження застосовували методи молекулярного стикування in silico. Відповідно до результатів, отриманих із програми стикування GOLD, ципрофлоксацин та моксифлоксацин зв’язуються з активним центром білка сильніше, ніж нативний ліганд. При порівнянні з позитивними контролями детальний аналіз взаємодій ліганд-білок показує, що досліджувані фторхінолони виявляють більшу кількість білкових взаємодій, ніж хлорохін та нелфінавір [28].
В іншому дослідженні науковці вивчали комбінацію противірусного препарату арбідол ( по 100 мг, тричі на день протягом 14 днів) та моксифлоксацином (0,4 г, один раз на день протягом 7-14 днів) у лікуванні важких пацієнтів з COVID-19 у відділеннях реанімації. Після лікування арбідолом та моксифлоксацином протягом одного тижня показники нуклеїнової кислоти SARS-CoV-2 становили 69,2% у досліджуваній групі та 77,8% у групі контролю.
ІЛ-6 визначався в обох групах і був вищий у групі спостереження, ніж контролю (р = 0,011). Після лікування арбідолом та моксифлоксацином протягом одного тижня ІЛ-6 значно знизився у групі спостереження (р = 0,023). Лікування арбідолом та моксифлоксацином призводило до зменшення вірусного навантаження та запалення під час інфекції SARS-CoV2. Однак дані дослідження ще продовжуються і чекають подальшої клінічної перевірки [29].
Статистика показує, що в середньому важкохворим дорослим пацієнтам із COVID-19 призначають антибіотики у 87-94% випадків. Залежно від країни застосування антибіотиків фторхінолонового ряду по всьому світу коливається від 50% до 92% [31]. Попередні спостереження показують, що левофлоксацин, ципрофлоксацин та моксифлоксацин, здається, є фторохінолонами вибору при їх використанні.
Згідно рекомендацій керівництва SSC ( Керівництво по лікуванню сепсису) по веденню дорослих пацієнтів в критичному стані внаслідок коронавірусної хвороби 2019 (COVID-19) до отримання результатів ПЛР-дослідження на SARS-CoV-2 і поки діагноз COVID-19 лабораторно не підтверджено, всіх пацієнтів з клінічною картиною важкої пневмонії і ГРДС слід вести як пацієнтів з гострою важкою позалікарняної пневмонією [32]. Слід негайно розпочати стартову емпіричну комбіновану антибактеріальну терапію (АБТ), оскільки відстрочене призначення антибіотиків на більш ніж 4 год статистично значимо підвищує ризик смерті таких пацієнтів [33].
Особливої уваги потребують до себе пацієнти віком ≥60 років з клінічною картиною COVID-19, які потребують госпіталізації і відносяться до групи високого ризику ускладнень і несприятливого результату в зв’язку з імунодефіцитом внаслідок будь-яких супутніх патологій: онкологічного захворювання або цукрового діабету, хронічної ниркової недостатності з необхідністю гемодіалізного лікування або системних захворювань сполучної тканини з необхідністю постійного прийому глюкокортикостероїдів, імунодепресантів. Для цих пацієнтів характерна асоціація збудників, 3/4 яких представлені сполученнями грампозитивної і грамнегативної флори.
Спектр мікробної флори у таких пацієнтів включає Streptococcus pneumoniae, Chlamydophila pneumoniae, Legionella spp., Haemophilus influenzae, грамнегативні ентеробактерії, Staphylococcus aureus і, досить рідко, Mycoplasma pneumoniae. Тому при підборі емпіричної терапії у літніх людей слід орієнтуватися на антибіотики, які ефективні при пневмококовій інфекції, при гемофільній паличці [33,34], а також при внутрішньоклітинних збудниках: Сhl. pneumoniae, Legionella spp., M. pneumoniae.
У зв’язку з цим слід звернути особливу увагу на такий препарат, як моксіфлоксацин. Враховуючи стійкість його молекулярної формули в організмі пацієнта, хорошу біодоступність з максимальною внутрішньоклітинною проникністю завдяки зв’язуванню з білками плазми крові, хорошу переносимість, мінімальна кількість побічних реакцій[34].
Беручи до уваги обмежені економічні ресурси галузі охорони здоров’я та нашої держави в цілому, звертає на себе увагу генерик препарату моксифлоксацин, а саме представлений на фармакологічному ринку препарат Максіцин («Юрія-Фарм», Україна).
Особливості застосування препарату Максіцин («Юрія-Фарм», Україна)
Препарат Максіцин містить всі необхідні репрезентативні характеристики антибіотика з оптимальним показником вартість / ефективність – є генеричним препаратом, прийнятний для проведення стартової парентеральної терапії, має високу ефективність і безпеку, володіє широким антибактеріальним спектром дії, активністю щодо резистентних штамів патогенів, низьким рівнем побічних реакцій, хорошою переносимість.
Випускається у вигляді концентрату для приготування інфузійного розчину 20 мг / мл у флаконі 20 мл, на відміну від оригінального препарату (розчин для інфузій 400 мг у флаконі 250 мл). Що значно зменшує вартість препарату, а також водно-електролітне навантаження при призначенні інфузійної терапії у реанімаційних пацієнтів.
Враховуючи сучасні тренди рестриктивної інфузійної терапії при пневмонії (рекомендації відповідно до протоколу лікування коронавірусної інфекції, резолюції телемостів лікування коронавірусних пневмоній) – Максіцин® від «Юрія-Фарм» вирішує проблему з об’ємом інфузії у таких хворих, що профілактує розвиток набряку легень.
Рекомендований режим дозування Максіцину 400 мг 1 раз на добу при будь-яких інфекційних ускладненнях.
Препарат вводять внутрішньовенно у вигляді інфузії тривалістю не менше 60 хв, попередньо розчинивши у перелічених нижче сумісними з ним розчинами: вода для ін’єкцій, розчин натрію хлориду 0,9 %, розчин глюкози 5 %, розчин глюкози 10 %, розчин глюкози 40 %, розчин ксиліту 20 %, розчин Рінгера, розчин Рінгера лактатний [35].
Суміш розчину препарату Максіцин® з вищенаведеними інфузійними розчинами залишається стабільною протягом 24 годин при кімнатній температурі [35].
Висока активність моксифлоксацину щодо більшості зазначених збудників, низька ймовірність розвитку антибіотикорезистентності зумовила включення препарату в міжнародні клінічні рекомендації і керівництва по лікуванню пацієнтів з позагоспітальною та внутрішньогоспітальною пневмонією.
Так, в рекомендаціях IDSA і АТS 2005 р по лікуванню нозокоміальної пневмонії моксифлоксацин розглядають як препарат вибору в якості емпіричної монотерапії у пацієнтів з раннім початком захворювання і невідомими факторами ризику полірезистентності патогенів, а також при встановленій етіології пннвмонії в разі виявлення резистентних штамів пневмокока (American Thoracic Society, Infectious Diseases Society of America, 2005) [30].
Висновки
Переконлива доказова база високої клінічної ефективності і безпеки застосування моксифлоксацину в терапії при важких клінічних формах позалікарняної і нозокоміальної пневмонії, а також включення даного препарату в міжнародні та національні клінічні рекомендації дозволяють розглядати його в якості оптимального вибору при лікуванні інфекційних ускладнень із середньотяжким і тяжким перебігом.
Крім того, в час пандемії COVID-19, антибіотикорезистентності та повсюдного використання антибіотиків, препарати класу фторхінолонів, зокрема моксифлоксацин, які володіють широким спектром дії та можливою противірусною дією є найбільш доступною альтернативою в якості лікування бактеріальних ускладнень вірусної пневмонії.
Враховуючи обмежені економічні ресурси нашої держави та довготривале лікування інфекційних ускладнень препарат Максіцин (Юрія-фарм), який випускається у вигляді концентрату для приготування інфузійного розчину 20 мг / мл у флаконі 20 мл дозволяє провести високоефективну антибактеріальну терапію відповідно до затверджених міжнародних та національних стандартів з максимальною для українських пацієнтів доступністю та можливістю оптимізації інфузійної терапії (якісно та кількісно).
Автори:
Дмитрієв Д.В., Назарчук О.А., Бабіна Ю.М., Вінницький Національний Медичний Університет ім.М.І.Пирогова, м.Вінниця
Література:
- Wiemken TL, Peyrani P, Ramirez JA. Global changes in the epidemiology of community-acquired pneumonia. Semin Respir Crit Care Med. 2012;33(3):213–219
- Polverino E, Torres MA. Community-acquired pneumonia. Minerva Anestesiol. 2011;77(2):196–211.
- Almirall J, Bolibar I, Vidal J, Sauca G, Coll P, Niklasson B, Bartolome M, Balanzo X. Epidemiology of community-acquired pneumonia in adults: a population-based study. Eur Respir J. 2000;15(4):757–763.
- Welte T, Torres A, Nathwani D. Clinical and economic burden of community-acquired pneumonia among adults in Europe. Thorax. 2012;67(1):71–79.
- Nair GB, Niederman MS. Community-acquired pneumonia: an unfinished battle. Med Clin North Am. 2011;95(6):1143–1161.
- Jackson ML, Neuzil KM, Thompson WW, Shay DK, Yu O, Hanson CA, Jackson LA. The burden of community-acquired pneumonia in seniors: results of a population-based study. Clin Infect Dis. 2004;39(11):1642–1650.
- Howard LS, Sillis M, Pasteur MC, Kamath AV, Harrison BD. Microbiological profile of community-acquired pneumonia in adults over the last 20 years. J Infect. 2005;50(2):107–113.
- Lieberman D, Schlaeffer F, Boldur I, Lieberman D, Horowitz S, Friedman MG, Leiononen M, Horovitz O. Multiple pathogens in adult patients admitted with community-acquired pneumonia: a one year prospective study of 346 consecutive patients. Thorax. 1996;51(2):179–184.
- Kuzman I, Bezlepko A, Kondova Topuzovska I, et al. Efficacy and safety of moxifloxacin in community acquired pneumonia: a prospective, multicenter, observational study (CAPRIVI). BMC Pulm Med. 2014;14:105. Published 2014 Jun 30. doi:10.1186/1471-2466-14-105
- Karampela I; Dalamaga M. Could respiratory fluoroquinolones, levofloxacin and moxifloxacin, prove to be beneficial as an adjunct treatment in COVID-19?. Archives of medical research, 2020, 51.7: 741-742.
- Hooper, D.C. Mode of Action of Fluoroquinolones. Drugs 58, 6–10 (1999). https://doi.org/10.2165/00003495-199958002-00002
- Tano E, Cars O, Lowdin E. Pharmacodynamic studies of moxifloxacin and erythromycin against intracellular Legionella pneumophila in an in vitro kinetic model. J Antimicrob Chemother. 2005;56:240–2.
- Pestova E, Millichap JJ, Noskin GA, et al. Intracellular targets of moxifloxacin: a comparison with other fluoroquinolones. J Antimicrob Chemother. 2000;45:583–90. [PubMed] [Google Scholar]
- Petitpretz P, Arvis P, Marel M, et al. Oral moxifloxacin vs high-dosage amoxicillin in the treatment of mild-to-moderate, community-acquired, suspected pneumococcal pneumonia in adults. Chest. 2001;119:185–95
- Soman A, Honeybourne D, Andrews J, et al. Concentrations of moxifloxacin in serum and pulmonary compartments following a single 400 mg oral dose in patients undergoing fibre-optic bronchoscopy. J Antimicrob Chemother. 1999;44:835–8.
- Capitano B, Mattoes HM, Shore E, et al. Steady-state intrapulmonary concentrations of moxifloxacin, levofloxacin, and azithromycin in older adults. Chest. 2004;125:965–73.
- Breilh D, Jougon J, Djabarouti S, et al. Diffusion of oral and intravenous 400 mg once-daily moxifloxacin into lung tissue at pharmacokinetic steady-state. J Chemother. 2003;15:558–62.
- Pea F, Pavan F, Lugatti E, et al. Pharmacokinetic and pharmaco-dynamic aspect of oral moxifloxacin 400 mg/day in elderly patients with acute exacerbation of chronic bronchitis. Clin Pharmacokinet. 2006;45:287–95.
- Balfour JA, Lamb HM. Moxifloxacin: a review of its clinical potential in the management of community-acquired respiratory tract infections. Drugs. 2000;59:115–39.
- Miravitlles M. Moxifloxacin in respiratory tract infections. Expert Opin Pharmacother. 2005;6:283–93
- Ball P, Stahlmann R, Kubin R, et al. Safety profile of oral and intravenous moxifloxacin: cumulative data from clinical trials and postmarketing studies. Clin Ther. 2004;26:940–50.
- Torres A, El-Ebiary M, Riquelme R, et al. Community-acquired pneumonia in the elderly. Semin Respir Infect. 1999;14:173–83
- Яковлев СВ. Моксифлоксацин при тяжелой внебольничной пневмонии: первая возможность монотерапии/Яковлев СВ. Пульмонология, 2002, З: 123.
- Finch R, Colins O, Kubin R, et al. Moxifloxacin IV/PO compared with amoxicillin/clavulanate IV/PO with or without clarithromycin in the treatment of community-acquired pneumonia. Clin Microbiol Infect 2001; 7 (Suppl 1): 167.
- Drummond M, Finch R, Duprat-Lomon I, et al. Superior outcomes with moxifloxacin IV/PO monotherapy compared to IV/PO amoxicillin/clavulanate +/- clarithromycin in the treatment of community-acquired pneumonia [Poster 864]. 41st Interscience Conference on Antimicrobial Agents and Chemotherapy, Chicago, USA, 16-19 December, 2001.
- Lemmen SW., Häfner H., Klik S., Lütticken R., & Zolldann, D. Comparison of the Bactericidal Activity of Moxifloxacin and Levofloxacin against Staphylococcus aureus, Staphylococcus epidermidis, Escherichia coli and Klebsiella pneumoniae. Chemotherapy. 2003; 49(1-2), 33–35. doi:10.1159/000069779
- Kuzman I et al. Efficacy and safety of moxifloxacin in community acquired pneumonia: a prospective, multicenter, observational study (CAPRIVI). BMC pulmonary medicine, 2014, 14.1: 1-14.
- Marciniec, K., Beberok, A., Pęcak, P. et al. Ciprofloxacin and moxifloxacin could interact with SARS-CoV-2 protease: preliminary in silico analysis. Pharmacol. Rep . 2020; 72, 1553–1561 https://doi.org/10.1007/s43440-020-00169-0
- YU, DONGSHAN, et al. Treatment with arbidol and moxifloxacin in ordinary and severe adult patients infected with COVID-19. MedRxiv, 2020.
- Mandell LA, Wunderink RG, Anzueto A, et al.; Infectious Diseases Society of America. American Thoracic Society. Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults. Clin Infect Dis 2007;44(Suppl 2):S27-72.
- Alberta Health Services, CO. “COVID-19 Scientific Advisory Group Rapid Response Report.” 2020.
- Alhazzani W., Møller M.H., Arabi Y.M. et al. Surviving Sepsis Campaign: guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID19). Intensive Care Med (2020). https://doi.org/10.1007/s00134-020-06022-5
- Негоспітальна пневмонія у дорослих осіб: етіологія, патогенез, класифікація, діагностика, антибактеріальна терапія та профілактики. Адаптована клінічна настанова, заснована на доказах. Уніфікований протокол надання медичної допомоги дорослим хворим на негоспітальну пневмонію: Вид-ня офіційне / Ю.І. Фещенко, К.О. Белослудцева, О.А. Голубовська та ін. – К., НАМН України, 2016. – 111 с. [Електронний ресурс]. – Режим доступу: http://www.ifp.kiev.ua/doc/staff/pneumonia_guidelines_2016.pdf
- Belforti R.K., Lagu T., Haessler S. et al. Association Between Initial Route of Fluoroquinolone Administration and Outcomes in Patients Hospitalized for Community-acquired Pneumonia // Clin Infect Dis. – 2016. – Vol. 63. – P. 1-9. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4901867/
- Федорова ОА. Моксифлоксацин: фармакоэкономические аспекты рациональной антибиотикотерапии. Український медичний часопис, 2014, 6: 110-113.






